- پویا ویژن وارد کننده مواد اولیه غذایی
- 02144357890
- 09122368819
- info@pouyavizhen.com
تعاملات هیدروفوبیک سوکرالوز با ساختارهای پروتئینی
سوکرالوز با ساختارهای پروتئینی
هدف از این مطالعه بررسی تعاملات هیدروفوبیک سوکرالوز با ساختارهای پروتئینی است. در ادامه همراه ما باشید تا شما را با جزئیات تعاملات هیدروفوبیک سوکرالوز آشنا کنیم.
معرفی سوکرالوز
سوکرالوز برخلاف سایر شیرین کننده های مصنوعی، هنگام گرم شدن پایدار است و بنابراین می تواند در غذاهای پخته و سرخ شده استفاده شود. FDA سوکرالوز را در سال ۱۹۹۸ تأیید کرد. این بررسی مشخصات جامعی برای سوکرالوز شامل پروفیل های فیزیکی، تحلیلی و ADME و روش های سنتز آن را ارائه می دهد.
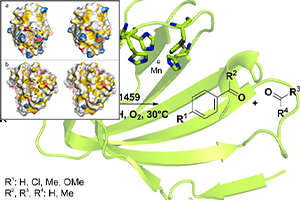
تعاملات هیدروفوبیک سوکرالوز با ساختارهای پروتئینی
سوکرالوز یک شیرین کننده مصنوعی متداول است که به نظر می رسد پروتئین را بی ثبات می کند. ساختارهای بومی این در تضاد مستقیم با طبیعت نگهدارنده زیستی همتای طبیعی آن، ساکارز است که ثبات مولکول های زیستی را در برابر فشار محیطی افزایش می دهد. ما بیشتر فعل و انفعالات مولکولی سوکرالوز را در مقایسه با ساکارز بررسی کرده ایم تا منشا تفاوت در اثر نگهدارنده زیستی آنها را روشن کنیم.
تحقیقات انجام شده نشان می دهد که حالت فعل و انفعالات سوکرالوز و ساکارز در محلول ها با استفاده از اندازه گیری دینامیک هیدراتاسیون و شبیه سازی محاسباتی به طرز ناخوشایندی متفاوت است. به نظر نمی رسد سوکرالوز حالت اصلی پروتئین ها را برای غلظت متوسط (<0.2 میلی متر) در دمای اتاق برهم بزند.
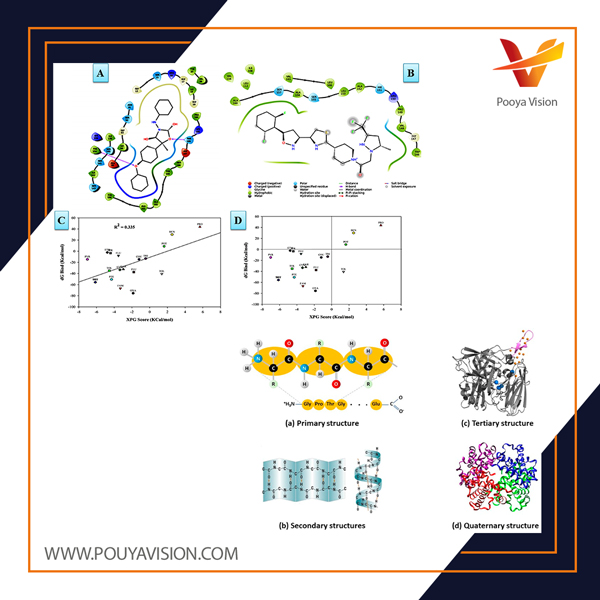
سوکرالوز یک اسمولیت کوچک مولکولی است که برای تنظیم ثبات ساختارهای پروتئینی محلول در برابر فشار محیطی مورد استفاده قرار می گیرد. دی ساکاریدها مانند ساکارز و ترهالوز قادر به محافظت از ارگانیسم های بیولوژیکی در برابر تنش های مختلف جسمی از جمله ذخیره سازی برودتی، افزایش درجه حرارت، کمبود آب و شوری بیش از حد هستند.
این موارد منجر به گسترش گسترده دی ساکاریدها در صنایع آرایشی، غذایی و دارویی شده است. از ویژگیهای زیست حفاظتی اسمولیتهای غیر کاهش دهنده ساکارید می توان به توانایی ساختار آب آنها از طریق حذف ترجیحی از رابط آب و پروتئین نسبت داد. ما قبلاً نشان دادیم، که هالوژناسیون ساکارز، برای تولید شیرین کننده مصنوعی سوکرالوز، منجر به کاهش اثر نگهداری بیولوژیکی ماده محلول می شود.
در حقیقت، در حالی که ساختار بومی پروتئین های مختلف تحت تأثیر حضور سوکرالوز برای غلظت های متوسط در دمای اتاق قرار نگرفت، پایداری در برابر تنش گرمایی به طور چشمگیری در حضور سوکرالوز کاهش یافت.
آنچه که باید راجب تعاملات هیدروفوبیک سوکرالوز و ساکارز با ساختارهای پروتئینی بدانید!
ساکارز به صورت وابسته به غلظت از حالت اصلی ساختارهای پروتئینی در برابر دناتوراسیون حرارتی محافظت می کند. ما دریافتیم که دمای ذوب هر دو استاف نوکلئاز و آلبومین سرم گاوی به طور خطی با غلظت ساکارز در محدوده ۰-۰٫۵M افزایش می یابد.
برخی دیگر نیز افزایش مشابه را در محدوده غلظت بیشتری گزارش کرده اند. در مقابل، ما دریافتیم که سوکرالوز به شدت وابسته به غلظت، دمای ذوب این سیستم های پروتئینی مدل را به شدت کاهش می دهد. به نظر می رسد که کاهش اثر حفظ انرژی زیستی ممکن است در اثر تغییر در خصوصیات الکترواستاتیک این مولکول باشد.
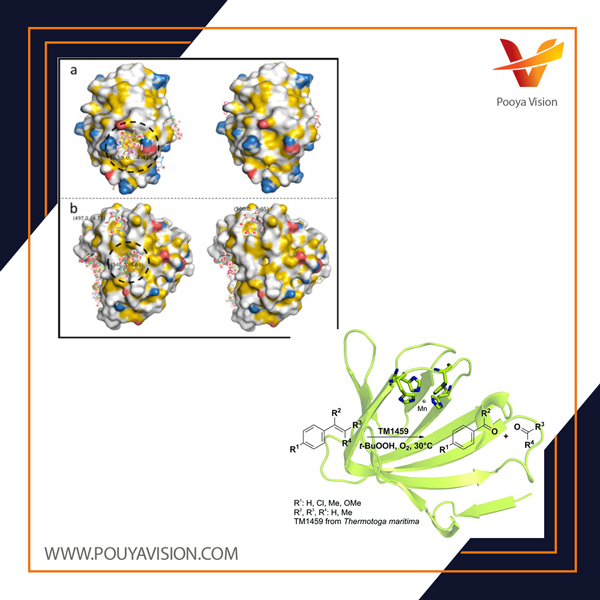
از آنجا که این امکان وجود دارد اتصال ساکارز و سوکرالوز به پروتئین ها تحت تأثیر میل آنها برای اتصال در محل فعال باشد، به منظور کاوش در کل سطح پروتئین، شبیه سازی ها به دو روش انجام شده است. فعالیت های مشاهده شده در ساختار بلوری رها شد و سپس دوباره با بستر حذف شده از محل فعال، شبیه سازی انجام شد.
ما ۱۰ هزار بار ساکرالوز و ساکارز را به تمام سیستم های پروتئینی مدل متصل کردیم. مشاهده کردیم که، به طور کلی، ساکارز و سوکرالوز به پروتئین هایی که میل ترکیبی کمتری نسبت به بسترهای آنها دارند، متصل می شوند. علاوه بر این، ما هیچ تفاوت معنی داری در حداقل یا میانگین انرژی اتصال ساکروالوز نسبت به ساکارز برای همه پروتئین ها مشاهده نکردیم.
این مشاهدات نشان می دهد که تفاوت بین سوکرالوز و ساکارز بسیار ظریف است، و احتمالاً به دلیل خاصیت خاص مکان های اتصال است.