- پویا ویژن وارد کننده مواد اولیه غذایی
- 02144357890
- 09122368819
- info@pouyavizhen.com
آسپارتام به عنوان یک همکار سابق در سیستمهای هممورف
آسپارتام به عنوان یک همکار سابق در سیستمهای هممورف
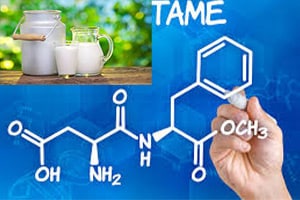
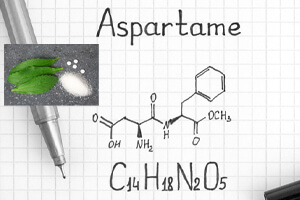
سیستمهای دارورسانی یک رویکردامیدوارکننده برای بهبود سرعت انحلال و بنابراین به طور بالقوه فراهمی زیستی خوراکی داروهای محلول در آب ضعیف است. چندین ماده جانبی با وزن مولکولی کم، به عنوان مثال اسیدهای آمینه، قبلاً نشان داده شده بود که فرم آمورف را تثبیت میکنند و سرعت انحلال داروها را افزایش میدهند. در این مطالعه، امکان سنجی آسپارتام، یک متیل استر از دی پپتید آسپارتیک اسید- فنیل آلانین، به عنوان یک سازنده مورد بررسی قرار گرفت و با اسیدهای آمینه منفرد مربوطه، به تنهایی و در ترکیب مقایسه شد.
همه مخلوطهای دارو و آسپارتام
ترکیبات بد محلول در آب مبندازول، تادالافیل و پیروکسیکام به عنوان داروهای مدل انتخاب شدند. برخلاف اسیدهای آمینه منفرد یا مخلوط فیزیکی هر دو، همه مخلوطهای دارو و آسپارتام پس از ۹۰ دقیقه آسیاب گلولهای بیشکل شدند. تنها یک دمای انتقال تک شیشهای (Tg) توسط کالریمتری اسکن تفاضلی مدوله شده تشخیص داده شد، که نشان میدهد یک سیستم همورف تک فازی همگن به دست آمده است. آزمایش انحلال پودر نشان داد که نرخ انحلال داروها از نمونههای هم آمورف دارو- آسپارتام در مقایسه با داروهای کریستالی افزایش یافته است.

علاوه بر این، فوق اشباع برای سیستمهای آمورف مبندازول-آسپارتام و تادالافیل-آسپارتام مشاهده شد. در نتیجه، نشان داده شده است که آسپارتام در سیستمهای هم آمورف یک سازنده امیدوارکننده است که نسبت به اسیدهای آمینه منفرد یا مخلوطهای آنها برتری دارد.حلالیت ضعیف بسیاری از داروها در آب یکی از چالشهای اصلی در تحقیق و توسعه دارویی است، زیرا اغلب منجر به جذب خوراکی کم و متغیر میشود و بنابراین دسترسی زیستی کم و اثرات درمانی رضایت بخشی ندارد.
انتقال یک داروی کریستالی و آسپارتام
یکی از روشهای شناخته شده برای افزایش سرعت انحلال و حلالیت ظاهری داروهای با محلول ضعیف در آب، انتقال یک داروی کریستالی به شکل آمورف آن است. اشکال اصلی استفاده از فرمولاسیونهای دارویی آمورف، پایداری فیزیکی ضعیف و تا حد زیادی غیرقابل پیشبینی آنها و خطر تبدیل آمورف-کریستالی در طول ساخت، ذخیرهسازی و تجویز است. بنابراین، یافتن راههای مناسب برای تثبیت داروهای آمورف در زمان ساخت و نگهداری ضروری است.
در سالهای اخیر، سیستمهای هم آمورف به عنوان یک جایگزین جالب برای پراکندگیهای جامد آمورف مبتنی بر پلیمر برای تثبیت داروهای آمورف ایجاد شدهاند. در مقایسه با پراکندگیهای جامد آمورف مبتنی بر پلیمر تودههای کمتری از مواد جانبی در سیستمهای هم آمورف به دلیل وزن مولکولی پایین مورد نیاز است. در سیستمهای آمورف دارو-اسید آمینه، مخلوط دوتایی دارو و اسید آمینه اغلب یک سیستم آمورف تک فازی همگن را تشکیل میدهد که از طریق فعل و انفعالات مولکولی، مانند پیوند هیدروژنی یا تشکیل نمک تثبیت میشود.

نشان داده شده است که برخی از آمینو اسیدها همسازکننده هایامیدوارکنندهای هستند و حضور اسیدهای آمینه سرعت انحلال ترکیب دارویی را افزایش داده و پایداری فیزیکی سیستم آمورف را در مقایسه با داروی معمولی تثبیت میکند. دو نکته کلیدی که آمینواسیدها یا سایر مواد جانبی را نویدبخش میسازد: همشکلپذیری خوب (یا تثبیت آمورف خوب) و افزایش انحلال. هم شکلپذیری خوب به این معنی است که همساز به راحتی با داروی داده شده سیستمهای هم آمورف تشکیل میدهد و فرم آمورف را برای مدت طولانی حفظ میکند، در حالی که افزایش انحلال خوب به این معنی است که سرعت انحلال یا/و حلالیت در آب دارو به طور قابل توجهی بهبود مییابد.
اسیدهای آمینه و بررسی آسپارتام
بر این اساس، همه اسیدهای آمینه همسازهای مناسب برای هر داروی داده شده نیستند. برخی از اسیدهای آمینه، مانند اسید آسپارتیک، گلوتامیک اسید، سرین، ترئونین، تیروزین، آلانین یا گلیسین، شکلپذیری ضعیفی از خود نشان دادند، یعنی بعید به نظر میرسد که به عنوان یک همساز عمل کنند و این به ویژگیهای قطبی آنها نسبت داده میشود. بنابراین، بررسی بیشتر راههای جایگزین یا اضافی برای تثبیت داروهای آمورف و بهبود رفتار انحلال آنها بر اساس مطالعات اسید آمینه قبلی، معنیدار است.
نتیجهگیری
در این مطالعه، امکان سنجی ASPA به عنوان همساز در سیستمهای هم آمورف همراه با سه داروی مدل مختلف MEB، TAD و PIR مورد بررسی قرار گرفت. نتایج نشان داد که همه مخلوطهای drugASPA پس از ۹۰ دقیقه آسیاب گلولهای به سیستمهای همآمورف و یک فاز تبدیل شدند، در حالی که مخلوطهای دوتایی دارو-اسید آمینه (دارو-ASP و دارو-PHE) و مخلوط سه تایی (دارو-ASPPHE) نشدند.
نرخ انحلال داروها به طور قابل توجهی از طریق تشکیل نمونههای همورف با ASPA افزایش یافت. نمونههای هم آمورف دارو-ASPA حداقل به مدت ۴ ماه در دمای ۲۵ درجه سانتی گراد و ۴۰ درجه سانتی گراد بیشکل باقی ماندند. این مطالعه نشان داد که ASPA در مقایسه با مخلوطهای ASP، PHE و ASP-PHE، یک کوفرمکننده بالقوهامیدوارکننده در سیستمهای هم آمورف است.